Mercure / Hg (HU) : Différence entre versions
(→Différentes sources de mercure dans l'environnement) |
|||
| Ligne 45 : | Ligne 45 : | ||
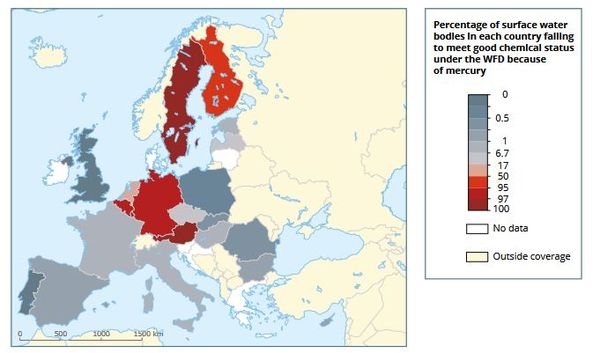
[[File:mercure_pollution_eau.JPG|600px|center|thumb|<center>''<u>Figure 4</u> : Pourcentage de masses d'eau par pays n'atteignant pas le bon état du fait de concentrations trop élevées en mercure ; <u>Source</u> : EEA (2018).''</center>]] | [[File:mercure_pollution_eau.JPG|600px|center|thumb|<center>''<u>Figure 4</u> : Pourcentage de masses d'eau par pays n'atteignant pas le bon état du fait de concentrations trop élevées en mercure ; <u>Source</u> : EEA (2018).''</center>]] | ||
| − | Au niveau mondial l'utilisation de mercure (provenant souvent du recyclage) pour l'orpaillage est une cause majeure de pollution dans les milieux aquatiques concernés. | + | Au niveau mondial l'utilisation de mercure (provenant souvent du recyclage) pour l'orpaillage est une cause majeure de pollution dans les milieux aquatiques concernés, par exemple en Guyanne. |
===Contribution des rejets d'assainissement=== | ===Contribution des rejets d'assainissement=== | ||
Version du 8 septembre 2022 à 16:14
Traduction anglaise : Mercury
Mot en chantier
Dernière mise à jour : 08/09/2022
Métal de symbole Hg et de numéro atomique 80 ; c'est le seul métal qui se présente sous forme liquide dans les conditions normales de température et de pression ; le mercure est extrêmement toxique, y compris sous sa forme métallique, ce qui justifie son classement parmi les métaux lourds.
Sommaire |
Nature et différentes formes physico-chimiques
Dans la nature, on trouve principalement le mercure sous forme de sulfures ; le sulfure de mercure (HgS), nommé cinabre en minéralogie, constitue son principal minerai. On trouve également du mercure métallique à l'état natif. Le mercure métallique est susceptible de s'oxyder dans l'air humide. Il existe alors deux niveaux d'oxydation :
- Le niveau 1 : ion mercureux Hg22+, par exemple Hg2SO4
- le niveau 2 : ion mercurique Hg2+, par exemple HgO, HgSO3, etc.
Outre sa très grande densité et son caractère liquide, le mercure présente l'intérêt de former des amalgames avec la plupart de métaux, et en particulier avec l'or et l'argent. Il est aussi extrêmement volatile, y compris sous sa forme métallique.
Sources et concentrations moyennes
Différentes sources de mercure dans l'environnement
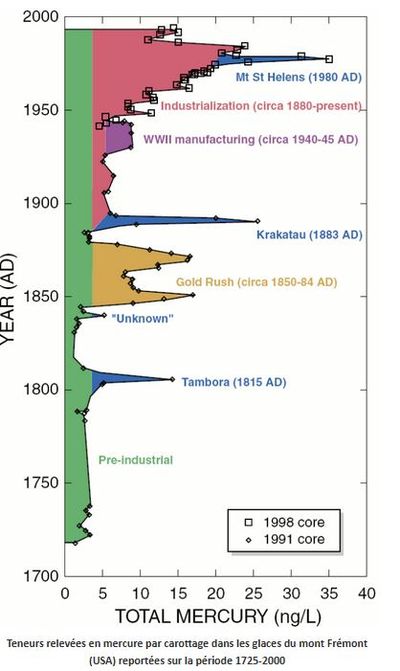
Le mercure est naturellement présent dans l'environnement, mais essentiellement dans les roches du sous-sol et ceci à de très faibles concentrations (entre 0,05 et 0,08 g/t). Ses principales sources naturelles dans l’environnement sont le dégazage de l’écorce terrestre et l’activité volcanique. Ces émissions naturelles sont estimées à 3 000 tonnes par an (Lindquist, 1991, cité par Bisson et al., 2010).
Les rejets anthropogéniques sont principalement dus à l’exploitation des minerais (mines de plomb et de zinc mais aussi exploitation des gisements d'or et d'argent), à la combustion des produits fossiles (principalement le charbon), aux rejets industriels (industrie du chlore et de la soude) et à l’incinération des déchets. La figure 1 permet de voir l'importance relative du dégazage naturel chronique (en vert), des pointes d'émission dues à l'activité volcanique (en bleu), de l'exploitation de l'or (en orange) et des autres sources industrielles à partir du XIXème siècle (figure 1). Cette figure montre également que le mercure, très volatile, se répand rapidement dans l'ensemble de l'atmosphère de la planète.
Les émissions anthropiques ont beaucoup baissé en France métropolitaine depuis le début du XXème siècle (figure 2). Cette baisse s’explique par l’amélioration des performances de l’incinération des déchets (mise en conformité progressive des usines d’incinération d’ordures ménagères (arrêtés du 25 janvier 1991 et du 20 septembre 2002), par la limitation ou l’interdiction de l’emploi de ce métal dans les piles et les thermomètres médicaux, par le tri des déchets, et enfin par l’optimisation des procédés de la production de chlore (www.citepa.org).
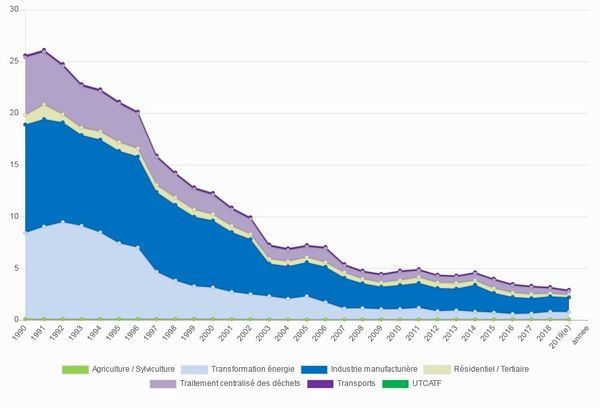
Cette baisse est plus faible au niveau européen et les émissions moyennes étaient, en 2018, de 103 mg par habitant et par an dans l’Union Européenne contre seulement 49 mg en France (EEA, 2018). Les émissions devraient continuer à diminuer dans les années à venir car toutes les utilisations industrielles du mercure sont maintenant interdites, excepté des amalgames dentaires. Il reste cependant d'importants stocks de mercure confiné (peintures, piles, thermomètres, etc.) qui sont progressivement relargués et ces émissions représenteraient 60% des émissions totales de la Communauté Européenne (EEA, 2018).
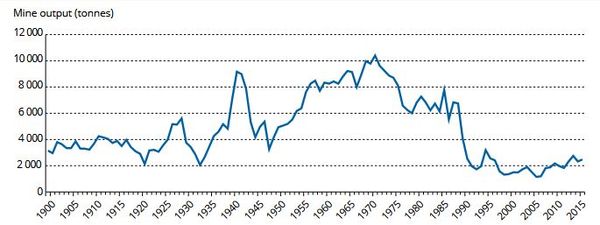
Au niveau mondial, la production a beaucoup baissé entre 1970 et 2000 mais elle a recommencé à augmenter depuis (figure 3). Elle est aujourd'hui d'environ 2 300 tonnes par an (www.planetoscope.com). On peut noter le lien direct entre la production mondiale annuel et les concentrations observées dans les carottes de glace (figure 1).
La diminution notable des émissions locales est cependant insuffisante car une part importante des apports est due à des dépôts atmosphériques ayant une origine extérieure à la CE (EEA, 2018). Ceci explique en partie pourquoi la concentration en mercure dans les eaux reste très importante dans la communauté européenne où le mercure est déclassant dans 46 000 masses d'eau de surface sur les 111 000 que compte le territoire (figure 3).
Nota : Les différences très importantes entre pays apparaissant sur la figure 3 sont en partie dues à des différences dans les protocoles d'évaluation (EEA, 2018).
Au niveau mondial l'utilisation de mercure (provenant souvent du recyclage) pour l'orpaillage est une cause majeure de pollution dans les milieux aquatiques concernés, par exemple en Guyanne.
Contribution des rejets d'assainissement
Lors du projet AMPERE (Coquery et al, 2011 et http://projetamperes.cemagref.fr/), les concentrations en mercure ont été mesurées à l'entrée et à la sortie de 21 stations d'épuration françaises. Les concentrations moyennes trouvées sont très variables mais se situent généralement dans la fourchette 0,1 à 1 μg/L, en entrée de station (eaux usées brutes) et de 0,01 à 0,1 μg/L en sortie après traitement secondaire. La masse rejetée aux milieux aquatiques a été estimée en moyenne à 1,8 μg/j/hab, soit une quarantaine de kg par an pour la France métropolitaine par an, ce qui est très faible.
Les quantités contenues dans les boues de station d'épuration sont plus importantes : comprises entre 1 et 10 mg/kg de matières sèche d'après Coquery et al. () ; ou égales en moyenne à 0,7 mg/kg de matière sèche d'après Amorce 2019, elles correspondent à un rejet d'environ 1 tonne par an.
Les concentrations en mercure dans les rejets urbains de temps de pluie ont été peu mesurés en France et très peu de données sont disponibles. Les concentrations semblent voisines de celles trouvés dans les eaux usées et l'apport des rejets de temps de pluie est probablement relativement faible.
Toxicité et danger associés
Impacts possibles sur la santé
Le mercure apparaît comme un puissant neurotoxique et reprotoxique sous ses formes organométalliques (monométhylmercure et diméthylmercure), de sels (calomel, cinabre, etc.) et sous sa forme liquide en elle-même. Chez l’homme, comme chez l’animal, le mercure métallique (Hg0) est essentiellement absorbé par voie pulmonaire du fait de sa très grande volatilité. Le mercure inorganique est pour sa part très peu absorbé par voie pulmonaire. De manière générale, chez l’homme, le mercure métallique et le mercure inorganique présentent un faible taux d’absorption par voie orale et encore plus faible par voie cutanée. Enfin, les sels mercuriques (Hg2+) sont plus facilement absorbés que les sels mercureux (Hg+). Le mercure organique, est absorbé plus facilement par voie orale.
Dans l'eau le danger principal est dû à sa capacité à se bioaccumuler dans les organismes et à se biomagnifier le long de la chaine alimentaire, en particulier sous la forme très toxique de méthyl-mercure. Bisson et al. (2010) proposent par exemple de retenir la valeur de 21 700 comme BCF poisson pour le mercure organique (figure 5).
Nota : Le facteur de bioconcentration (BCF) est le rapport entre la concentration du composé dans l’organisme et sa concentration dans l’eau.
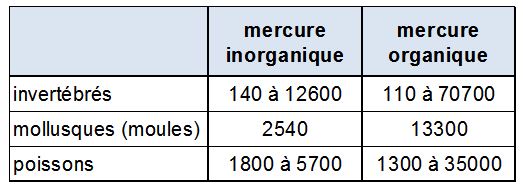
La consommation de poissons ou de coquillages contaminés constitue donc un danger important. Dans les années 1950, l'accident de Minamata au Japon, provoqué par la consommation de poissons contaminés, a fait 45 morts et des centaines d’handicapés. Depuis cette accident la pollution par le mercure est largement médiatisée et connue. Malgré tout, en 2021, il serait encore dans le monde la cause de 250 000 cas de déficience intellectuelle par an8, principalement via l'ingestion de produits de la mer (Liu et al., 2021). La limite de concentration dans les poissons est en général de 0,5mg/kg ; elle est portée à 1mg par kg pour certains prédateurs (EEA, 2018). Ces concentrations sont souvent dépassées, en particulier dans la Méditerranée, mer où les poissons sont les plus contaminés (figure 6).
La limite de concentration pour l'eau destinée à la consommation humaine est de 1μg/L.
Impacts possibles sur les milieux aquatiques
Le mercure minéral, très dense, se dépose rapidement dans les sédiments où il est transformé en méthyl-mercure par des bactéries. Le diméthyl-mercure gazeux diffuse dans l'atmosphère et le monométhyl-mercure est incorporé dans la chaine alimentaire où il se concentre par bioaccumulation. En 2018, l'Agence européenne de l'Environnement indiquait que "Près de 46.000 masses d'eau de surface dans l'UE, sur environ 111.000, ne respectent pas les niveaux de mercure fixés pour protéger les oiseaux et les mammifères piscivores".
Les valeurs de concentrations sans effet observé (NOEC pour No Observable Effect Concentration), de Valeur guide environnementale (VGE) (concentration moyenne annuelle dans l'eau) et de concentration maximale admissible (MAC pour Maximum Admissible Concentration) sont données dans le tableau de la figure 7 pour les eaux douces et marines. Les valeurs de VGE et de MAC, beaucoup plus faibles que les NOEC, sont justifiées par la grande capacité de bioaccumulation du mercure et la nécessite de protéger la santé humaine.

Globalement les risques présentés par la présence de mercure dans l'eau sont aussi plus importants pour la santé humaine que pour les écosystèmes aquatiques et leur gestrion constitue l'un des enjeux importants de gestion de la qualité des milieux aquatiques.
Bibliographie :
- Amorce (2019) : Quelles solutions pour valoriser les boues d’épuration ? ; Réf AMORCE EAT05 a ; 45p. ; disponible sur https://amorce.asso.fr/publications/quelles-solutions-pour-valoriser-les-boues-d-epuration-eat05
- Coquery M., Pomiès M., Martin-Ruel S., Budzinski H., Miège C., Esperanza M., Soulier C., Choubert J.-M.(2011) : Mesurer les micropolluants dans les eaux brutes et traitées - Protocoles et résultats pour l'analyse des concentrations et des flux ; Techniques Sciences et Méthodes, 1/2 : 25-43 ; disponible sur : projetamperes.cemagref.fr
- CGDD (2019) : La contamination des sols par les métaux ; Conseil Général au Développement Durable ; disponbible sur : www.notre-environnement.gouv.fr
- Desportes I. (coord.) (2007) : Bilan des flux de contaminants entrant sur les sols agricoles de France métropolitaine ; étude ADEME-SOGREAH ; rapport final ; 330p. ; disponible sur le site de l'ADEME.
- Lindquist, J.A. (1991) : Medium and Procedure for the Direct, Selective Isolation of Edwardsiella tarda from Environmental Water ; Poster presented at ASM Meeting in Dallas on May 8, 1991. AmSoc Microbiol, C-303, 302
- Liu, M., Zhang, Q., Maavara, T., Liu, S. (2021) : Rivers as the largest source of mercury to coastal oceans worldwide ; Nature Geoscience ; vol. 14, no 9, septembre 2021, p. 672–677 ; disponible sur www.nature.com.
Pour en savoir plus :
- Bisson, M., Vincent, J-M., Houeix, N., Diderich, R., Magaud, H. (2010) : Le mercure et ses dérivées ; fiche de données toxicologiques et environnementales ; INERIS ; 120p. ; disponible sur le Portail substances chimiques de l'INERIS.
- EEA (2018) : Mercury in Europe’s environment, a priority for European and global action ; rapport N°11-2018 ; European Environment Agency ; 72p. ; disponible sur www.eea.europa.eu.
 S'abonner à un flux RSS
S'abonner à un flux RSS